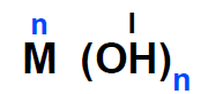O WODOROTLENKACH OGÓLNIE
Wodorotlenki - są to takie związki chemiczne, których cząsteczki składają się z;
Wodorotlenki - są to takie związki chemiczne, których cząsteczki składają się z;
- atomu metalu lub grupy amonowej
- grupy wodorotlenkowej
Me:atom metalu
OH: grupa wodorotlenkowa - jest zawsze I wartościowa, składa się z jednego atomu wodoru i jednego atomu tlenu
n: jest to liczba, która określa nam wartościowość metalu i jednocześnie informuje o liczbie grup wodorotlenkowych w cząsteczce danego wodorotlenku.
WODOROTLENEK WAPNIA JAKO PRZEDSTAWICIEL WĘGLOWODORÓW
1. wzór sumaryczny
Ca(OH)2
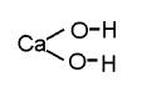
2. wzór strukturalny
OH: grupa wodorotlenkowa - jest zawsze I wartościowa, składa się z jednego atomu wodoru i jednego atomu tlenu
n: jest to liczba, która określa nam wartościowość metalu i jednocześnie informuje o liczbie grup wodorotlenkowych w cząsteczce danego wodorotlenku.
WODOROTLENEK WAPNIA JAKO PRZEDSTAWICIEL WĘGLOWODORÓW
1. wzór sumaryczny
Ca(OH)2
2. wzór strukturalny
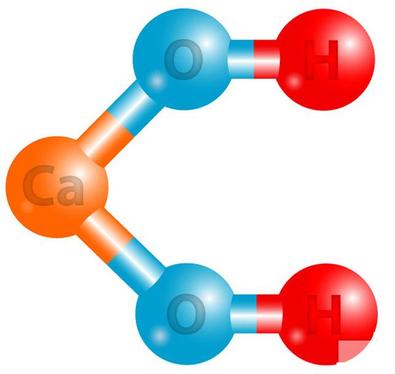
3. model cząsteczki
4. Właściwości:
7. Zastosowania:
6. Ważne pojęcia:
DYSOCJACJA JONOWA ZASAD
Zasady - są to wodorotlenki, które są bardzo dobrze i dobrze rozpuszczane w wodzie. Zasadami są np; zasada sodowa, zasada potasowa, zasada wapniowa.
Dysocjacja jonowa zasad - polega na rozpadzie zasad pod wpływem wody na;
H20
Me(OH) -------------> Me+ + OH-
Me+ - kationy metalu
OH- - aniony wodorotlenkowe
w tym filmiku wytłumaczone jest jak prosto rozwiązywać reakcje dysocjacji jonowej zasad
- chemiczne: wodorotlenek, żrący
- fizyczne: substancja stała, barwy białej, trudno rozpuszczalna w wodzie
- reakcja wapnia w wodą: Ca + 2H2O -> Ca(OH)2 + H2↑
- reakcja tlenku wapnia z wodą: CaO + H2O -> Ca(OH)2
7. Zastosowania:
- budownictwo
- sadownictwo
- dezynfekcja pomieszczeń sanitarnych
- produkcja przetworów i karmy dla zwierząt
- w garbarstwie stosowane do usuwania włosów ze skór
6. Ważne pojęcia:
- wapno palone, czyli tlenek wapnia - to substancja stała, barwy białej, trudno rozpuszczalna w wodzie, która powstaje w wyniku rozkładu wapieni.
- wapno gaszone, czyli wodorotlenek wapnia - to substancja żrąca, barwy białej, która powstaje w wyniku gaszenia wapna palonego
- zaprawa wapienna - powstaje po zmieszaniu wodorotlenku wapnia, czyli wapna gaszonego z piaskiem oraz wodą
- woda wapienna - jest to nasycony roztwór wodorotlenku wapnia. Służy do wykrywania obecności dwutlenku węgla. Pod jego wpływem robi się biała.
- mleko wapienne - jest to zawiesina wodorotlenku wapnia w wodzie - wykorzystywana w sadownictwie do bielenia drzewek.
DYSOCJACJA JONOWA ZASAD
Zasady - są to wodorotlenki, które są bardzo dobrze i dobrze rozpuszczane w wodzie. Zasadami są np; zasada sodowa, zasada potasowa, zasada wapniowa.
Dysocjacja jonowa zasad - polega na rozpadzie zasad pod wpływem wody na;
- kationy metalu
- aniony wodorotlenkowe
H20
Me(OH) -------------> Me+ + OH-
Me+ - kationy metalu
OH- - aniony wodorotlenkowe
w tym filmiku wytłumaczone jest jak prosto rozwiązywać reakcje dysocjacji jonowej zasad
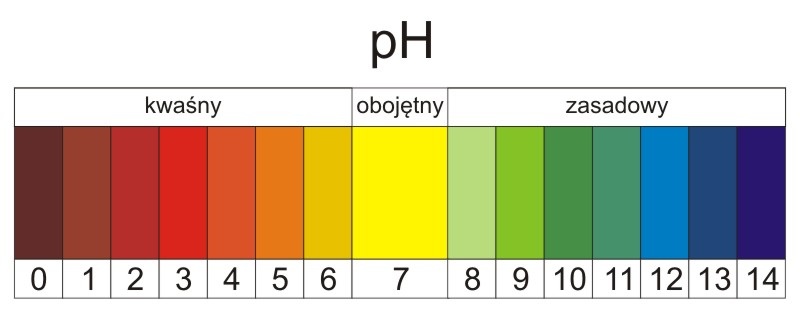
ODCZYN ROZTWORU - SKALA pH
Odczyn roztworu - to cecha charakterystyczna dla danego roztworu, która określa nam, czy w roztworze znajduje się nadmiar jonów wodoru, czy nadmiar janów wodorotlenkowych lub czy stężenia tych jonów są sobie równe. Odczyn roztworu dzielimy na trzy rodzaje;
Odczyn roztworu - to cecha charakterystyczna dla danego roztworu, która określa nam, czy w roztworze znajduje się nadmiar jonów wodoru, czy nadmiar janów wodorotlenkowych lub czy stężenia tych jonów są sobie równe. Odczyn roztworu dzielimy na trzy rodzaje;
- odczyn kwasowy - przewaga jonów wodorowych
- odczyn obojętny (czyli neutralny) - stężenie jonów wodorowych i wodorotlenkowych są sobie równe
- odczyn zasadowy - przewaga jonów wodorotlenkowych
- fenoloftaleina (wykrywa zasady)
- oranż metylowy (wykrywa kwasy)
- uniwersalne papierki wskaźnikowe (wykrywa zasady i kwasy)